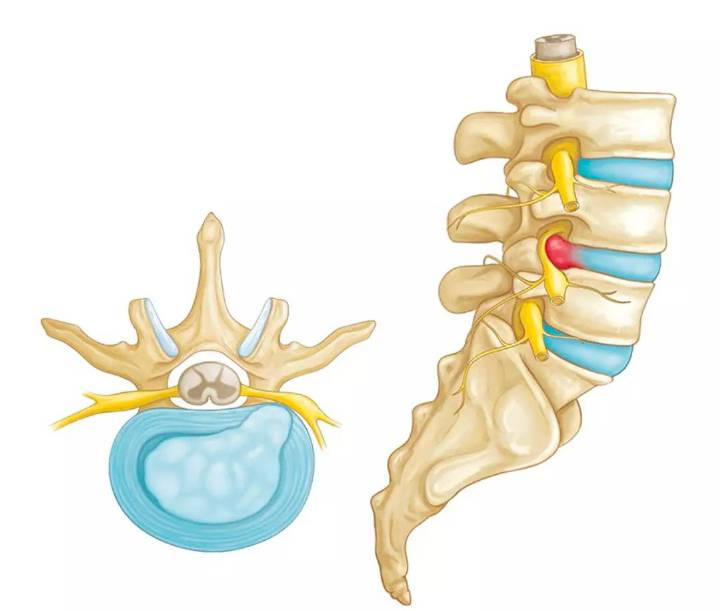
腰椎间盘突出症(lumbar disc herniation,LDH)已成为我国临床常见多发疾病之一。目前认为LDH基本病理改变为椎间盘的退变,然而椎间盘退行性变(intervertebral disc degeneration,IDD)的主要病因和其发病机制尚未明确,也无适宜的治疗措施。动物模型研究是应用于生物医学科技研究中的一种重要工具,针对特定疾病设计对应的动物模型,通过动物模型进行研究动物发病机制与检测验证诊断治疗的有效性,在临床研究中具有无法替代的优势和作用。
动物的选择
目前最常用的是大鼠模型,饲养方便、价格便宜、繁殖迅速,最重要的是其椎间盘解剖结构与人类椎间盘结构极为相似。
近年来,也有研究者选用兔、羊、猪等动物制备IDD动物模型。
灵长类动物无论在进化方式或解剖结构方面来说均与人类最为相似,如恒河猴,是目前为止最理想的动物模型,但由于经济方面的制约不能大量的应用。
造模方法
一、直接结构损伤模型
01纤维环损伤模型
纤维环模型是目前最常用的动物模型。
造模方法:研究者选取兔,利用各种规格不同的穿刺针(16、18、21g)在兔子的纤维环上进行穿刺,构建一种可令MRI分级及椎间盘高度均有所下降的IDD 模型。将两种不同尺寸和规格的针头进行对照,通过结构学和影像图形学的研究和观察,以25g针头作为对照,21g针头所引起的椎间盘退变更加严重,且椎间盘突出的发生率与针头的大小呈正比。
优缺点:这种穿刺纤维致使结构破坏的造模方法周期短、可行性高、操作简易,但创伤大、易感染、损伤程度各异等缺点也很明显。经皮穿刺纤维法虽可弥补这方面的不足,但是盲穿难度大,需要C臂机进行配合。
02终板损伤模型
该模型通常采用钻孔方式破坏终板结构,由椎体斜穿一个孔洞直达终板和髓核。
造模方法:研究者选取家猪,通过穿刺家猪的椎体终板,3个月后在T2加权像磁共振下发现纤维环水份和蛋白多糖含量明显减少。
03化学损伤模型
造模方法:研究者选取兔,在兔腰椎间盘注射纤维连接蛋白片段,8~16 周后聚集蛋白聚糖和Ⅱ型胶原mRNA表达明显下调。
二、机械间接损伤型模型
01机械应力型模型
机械负荷是引起IDD的重要因素之一。
造模方法:有研究者选取兔,聚氯乙烯管将兔双腿固定于直立位,8周后,MRI显示椎间盘高度指数下降,T2加权信号降低,证明IDD的程度与椎间盘应力变化有关。
优缺点:该模型操作简单、损伤小、易获得,且高度类似人体正常行走的状态,但所需时间长,成功率低,只能用于小型动物。
02椎体不稳的造模
此类造模技术主要是通过使用手术方法损伤关节面或者棘突等所能支持的组织,反复不断地对局部的脊柱和肌肉进行一定的刺激,从而导致椎间盘受力不平衡达到IDD的方法。
造模方法:有研究者利用手术横向切除羊脊柱后部棘突等支撑性组织,模型组随后即出现了椎间隙狭窄、髓核纤维化等IDD的表现。
03自发模型
选取沙鼠为试验动物。
沙鼠以含盐量较高的灌木为食,IDD有显著的遗传性。其中大多数18~30个月龄沙鼠在椎间盘内可以同时发现纤维骨赘环囊性生长改变、裂隙和纤维骨赘囊性生长,并有纤维环膨出和髓核突入终板。沙鼠的饮食习惯(高盐低水)一定程度影响了代谢情况,从而引起了 IDD的发生,尤其特别是对于髓鞘单核细胞功能异常性的改变。
有研究者发现10%的沙鼠动物细胞IDD改变发生在3个月,而50%的沙鼠动物则可能会逐渐发生一次性细胞退化改变在5个月。
总结
IDD是随着年龄的不断增长而出现的复杂的退行性变化,以目前的情况而言,构建完全与该退变相同的动物模型十分困难。且动物和人类的生活方式、解剖生理及病理差异使该模型更加复杂。IDD模型通常会造成椎间盘及附属器件出现各种形态学的变化,使方法、变化程度及时间也不同。虽然,动物造模所能提供的 IDD 信息存在局限性,但相比于直接研究人类IDD时间要短得多,且更具有操控性和选择性。

