资源中心
Ramelteon改善血脑屏障(BBB)的高渗透性
时间:2021-10-13 02:10:00点击量:1526次
摘要:血脑屏障(BBB)通过选择性地交换血液和大脑之间的物质来保护脑组织。BBB的完整性可能会受到多种因素的破坏,包括氧化应激和炎症。Ramelteon是一种口服催眠药,在本研究中,研究了其对BBB损伤的保护作用及其潜在机制。LPS用于诱导小鼠BBB损伤并刺激内皮细胞损伤。伊文思蓝染色测定用于测量脑通透性。分别使用免疫染色和蛋白质印迹在脑组织和内皮细胞中评估ZO-1和Occludin的表达。qRT-PCR和ELISA用于检测脑血管中IL-1β和MCP-1的产生。TBA测定用于检查脑组织和内皮细胞中MDA的浓度。使用蛋白质印迹法测定细胞核中Nrf2和NQO1的表达。使用FITC-葡聚糖渗透测定检查单层的内皮渗透性。首先,用Ramelteon治疗显着逆转了由LPS诱导的脑组织中脑通透性增加和紧密连接蛋白表达下调,伴随着小鼠血管中IL-1β和MCP-1的产生减少。此外,通过用Ramelteon治疗,Nrf2信号被激活,脑血管中的氧化应激得到缓解。其次,LPS诱导内皮单层通透性增加,bEnd中紧密连接蛋白表达减少。3脑内皮细胞被Ramelteon显着逆转,伴随着激活的Nrf2信号和减轻氧化应激。最后,Ramelteon对LPS诱导的ZO-1和Occludin减少以及内皮单层渗透性增加的保护作用通过沉默Nrf2显着消除。Ramelteon可能通过激活Nrf2信号通路来改善LPS诱导的BBB的高渗透性。
血脑屏障(BBB)通过选择性地在脑实质和血液之间转移物质,在保护脑组织方面发挥着重要作用。其损伤与脑卒中、血管认知、阿尔茨海默病、脑损伤等多种疾病的发病机制有关。LPS已被证明可激活NADPH氧化酶并诱导过量ROS的产生,这进一步导致BBB完整性的破坏。当LPS诱导的ROS排泄和消除平衡被打破时,ROS过度积累引起氧化应激,参与BBB完整性受损引发的疾病的发病机制。通过抑制氧化应激的过程,降解的紧密连接蛋白和受损的BBB得到显着逆转。因此,氧化应激可能是保护BBB完整性和治疗相关疾病的一个有希望的目标。
Ramelteon是一种口服催眠药,作为第一个用于治疗失眠症的黑色素瘤受体激动剂,已经报道了对棘手、慢性和急性失眠症的有希望的治疗效果。最近有报道称,Ramelteon通过改善氧化应激和炎症对创伤性脑损伤发挥脑保护作用,以及对异氟醚诱导的脑微血管内皮细胞炎症的抑制作用。在本研究中,本文作者研究了Ramelteon对BBB完整性的保护作用,旨在探索Ramelteon对神经退行性疾病的潜在治疗特性。
方法与结果
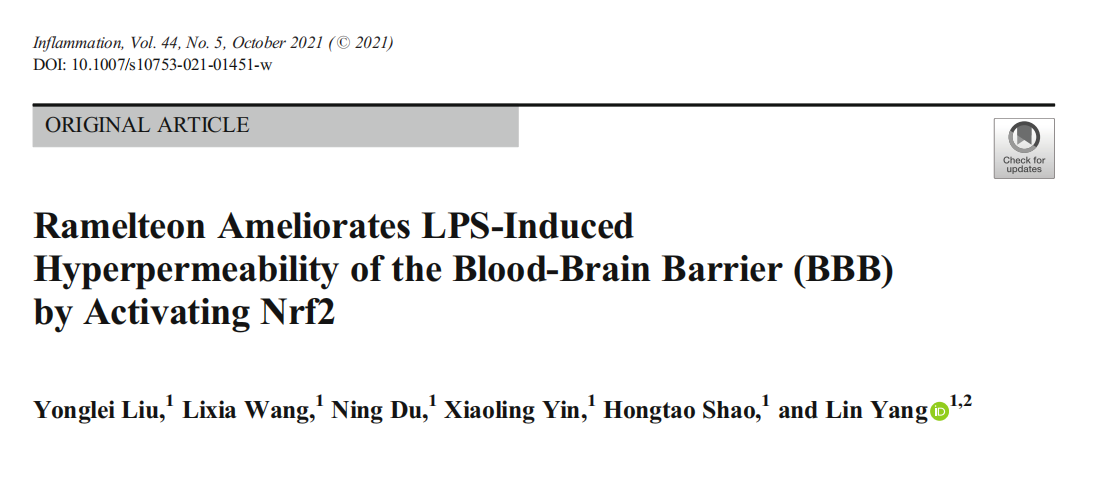
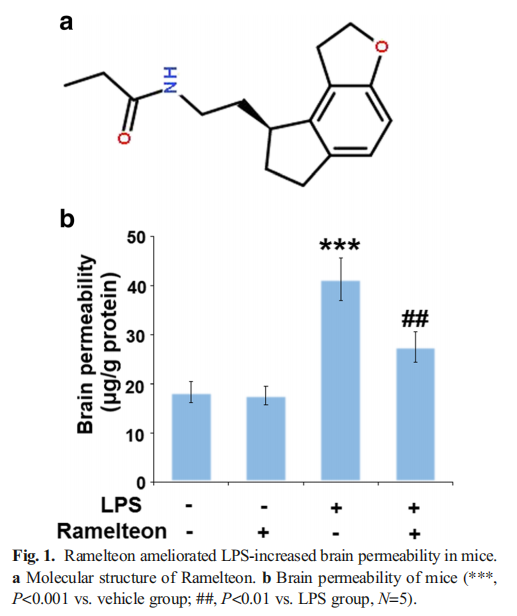
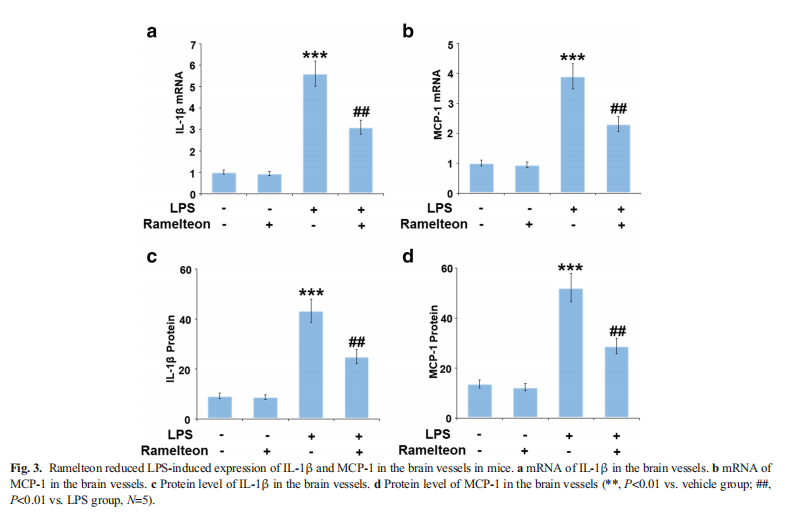
本研究利用LPS 诱导小鼠 BBB 损伤并刺激内皮细胞损伤。结果显示,Ramelteon改善了LPS增加的小鼠脑通透性(见图一);Ramelteon改善了LPS诱导的小鼠脑中ZO-1和Occludin的减少(见图二),降低LPS诱导的小鼠血管中IL-1β和MCP-1的表达(见图三)。进一步研究结果显示,Ramelteon激活Nrf2信号并减轻小鼠血管中的氧化应激(见图四);Ramelteon在bEnd.3脑内皮细胞中防止LPS增加的内皮渗透性和细胞死亡(见图五);Ramelteon阻止了LPS诱导的bEnd.3脑内皮细胞中ZO-1和Occludin的减少(见图六),激活了Nrf2信号并减轻bEnd.3脑内皮细胞的氧化应激(见图七)。Nrf2的沉默消除了Ramelteon对LPS诱导的ZO-1和Occludin减少以及内皮单层渗透性增加的保护作用(见图八)。

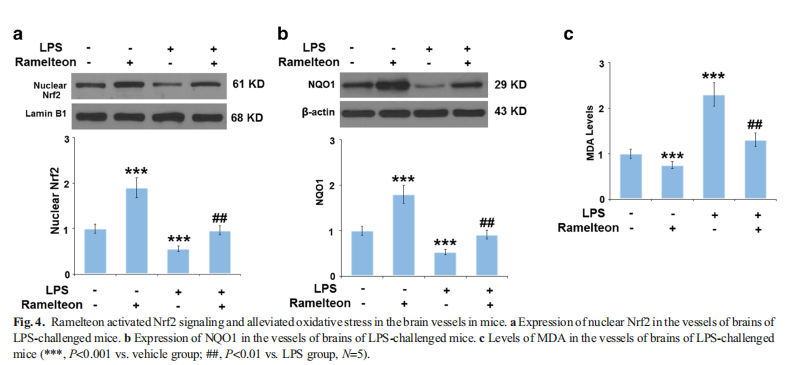


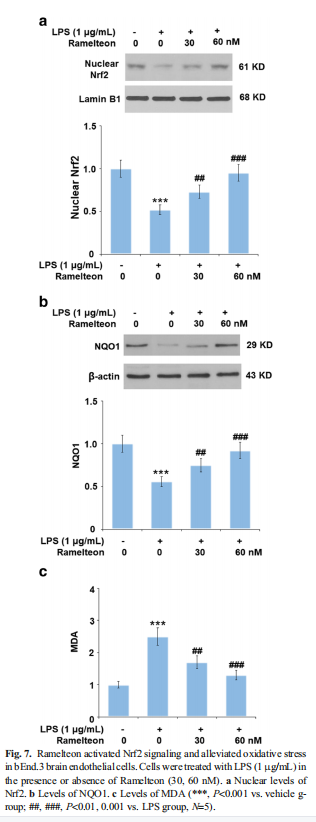
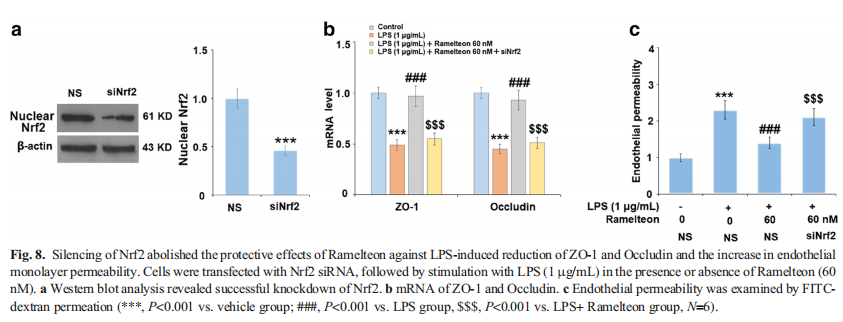
本研究实验数据表明Ramelteon可能通过激活Nrf2信号通路来改善LPS诱导的BBB的高渗透性。
在未来的研究工作中,可以引入Nrf2抑制剂来验证Ramelteon在动物模型中对BBB的保护作用的机制,为Ramelteon在退行性疾病中的潜在应用提供更多证据。



