样品准备:实验第一步是准备样品。如果是贴壁细胞,先把爬片在70%乙醇里泡一会儿消毒,再用无菌镊子夹到培养皿里,用无菌PBS洗洗残留乙醇,然后把细胞接种到爬片上,过夜培养,等细胞长成单层,小心取出爬片就行。要是细胞不小心脱落,实验就得重来。悬浮细胞则要提前处理爬片,让细胞能贴壁,一般几小时就行,后续接种操作和贴壁细胞一样。
固定:固定细胞常用的甲醛浓度是2% - 4%,室温下固定20分钟左右。比如用4%多聚甲醛固定爬片15分钟,再用PBS浸洗3次,每次3分钟,洗掉多余固定剂。但如果实验用到磷酸化抗体,甲醛可能会让磷酸蛋白从细胞膜表面跑到胞浆里,这时候就得用冰冷的无水甲醇或无水乙醇来固定。
通透:这一步是为了让抗体能进入细胞内部。用0.5% Triton X - 100(用PBS配制),室温处理20分钟,就能在细胞膜上开个小通道。如果目标抗原就在细胞膜上,这步就可以省略。
封闭:通透后,先用PBS浸洗3次,每次3分钟,再用吸水纸吸干PBS,然后选好封闭液,常用的有和二抗同一来源的血清、BSA或羊血清。室温封闭60分钟,从这一步开始,要注意保持样品湿润,否则背景信号会升高,影响实验结果。
一抗孵育:按一抗说明书,用一抗稀释液稀释好一抗,吸尽封闭液后,滴加到每张玻片上,放进湿盒,4℃孵育过夜。第二天回收一抗,用PBST洗涤3次,每次5分钟,洗掉未结合的一抗。一抗可以回收,在-20℃保存,一般能重复使用3次左右,具体看抗体的灵敏度。
荧光二抗孵育:吸尽洗涤液后,滴加稀释好的荧光二抗,湿盒里孵育1小时。回收二抗,用PBST洗3次,每次5分钟。从加荧光二抗开始,后面操作都要避光,防止荧光淬灭。二抗孵育时间通常1 - 2小时,常温操作。选择二抗时,不能和一抗属性相同,否则容易串色。洗涤时,一抗用PBS洗,二抗用TBST,适当增加吐温浓度,洗涤效果更好。
复染核:在玻片上滴加DAPI,避光孵育5分钟,给细胞核染色。然后用PBST洗3次,每次5分钟,洗掉多余DAPI,这样就能清晰区分细胞核和其他细胞结构。
封片及荧光观察:用吸水纸吸干爬片上的液体,用含抗荧光淬灭剂的封片液封片,最后在荧光显微镜下观察,记录实验结果。
免疫荧光实验中串色问题解析
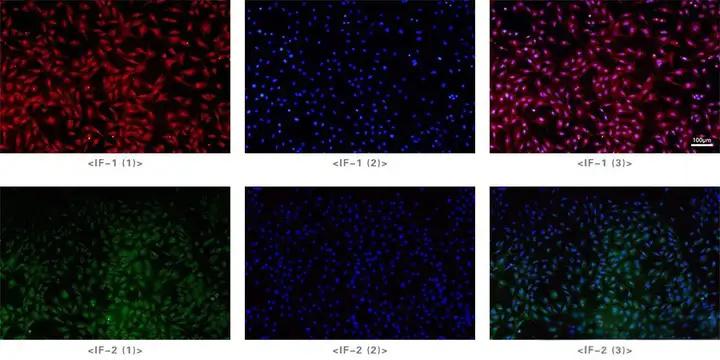
在免疫荧光实验里,串色问题特别烦人。串色,简单说就是多重荧光染色时,不同荧光染料的信号混到一块儿,分不清彼此。这就跟音乐会一样,每个乐器都有自己的声音,要是混成一团,旋律就乱了,实验结果也跟着出错。
想想看,你辛辛苦苦做实验,想看看两个蛋白是不是挨在一起,结果因为串色,把本来不在一起的蛋白误以为是共定位,还据此得出错误结论,那前面的努力不就白费了?串色直接影响荧光信号的纯度,对实验结果的准确性影响特别大,必须重视起来!
避免串色的实用 Tips
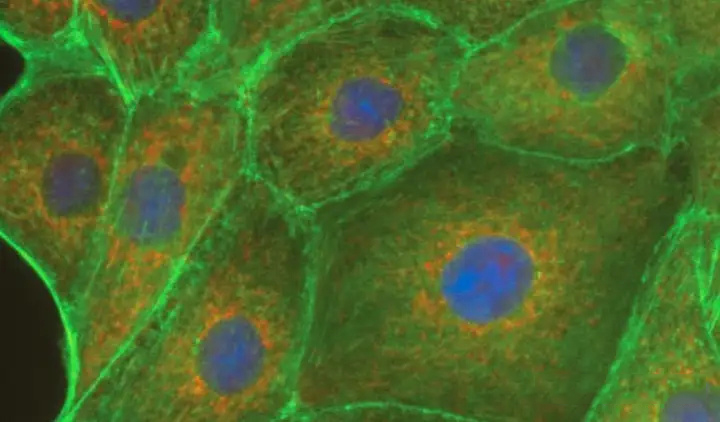
细胞准备注意事项
细胞铺板时,密度一定要控制好。铺得太密,一抗结合位点太多,非特异性染色的风险就高,还会影响拍摄效果。比如,从6孔板取1/8的细胞量铺到12孔板里,培养12小时左右,密度就比较合适,能有效减少串色风险。在细胞种类选择上,大体积细胞(如HeLa细胞)拍摄效果更好,而HEK细胞稍差一些。不过,如果用非工具细胞,就不用太纠结细胞体积了。细胞状态也很关键,健康的细胞染色效果好,要是细胞被支原体污染,会出现严重的非特异性染色,甚至核染色和抗体染色都会异常。所以实验前一定要做好支原体清除工作。
抗体使用要点
抗体的正确使用是避免串色的关键。研究外源蛋白时,用标签抗体,特异性高,用量少,一般1:500左右就行。如果是染内源性蛋白,一抗浓度可以提高到1:200左右,但一定要仔细查阅抗体说明书,确认它是否适合免疫荧光实验。一抗孵育时,4℃过夜孵育能让抗体和抗原充分结合,效果更好。一抗还能回收,在-20℃保存,一般能重复使用3次左右。在双抗体免疫荧光实验中,抗体组合很重要,要选不同宿主来源的抗体,比如一个小鼠抗体,一个兔抗体,千万别选双小鼠或双兔抗体,不然容易交叉反应导致串色。二抗孵育时间一般1 - 2小时,常温进行,注意避光。选择二抗时,别和一抗属性相同,否则容易串色。洗涤时,一抗用PBS洗,二抗用TBST(TBS + 0.05% Tween - 20),适当增加吐温浓度,能把没结合的二抗洗得更干净,减少串色。
染色与拍摄技巧
染色顺序也很重要。在双抗体染色实验里,核染色要放在最后一步。别在实验一开始就用活细胞染核液(如Hoechst),而是在封片时用DAPI进行核染色,同时要控制好DAPI的浓度,低浓度就能达到不错的效果,浓度太高容易串色。拍摄时,激发光的选择是避免串色的最后一道防线。封片后拍摄,要选没有交叉波长的激发光,比如绿光488 nm和红光555 nm,这样能让不同荧光信号互不干扰,清晰捕捉到每个荧光信号,得到准确的实验结果。
实验中的其他常见问题与解决办法
在免疫荧光实验里,串色只是个麻烦事,其他问题也常冒出来添乱。比如信号弱,可能是因为抗体浓度过低、抗原表达量少,或者抗原修复不充分。这时候就得调整抗体浓度、检查样品质量,或者优化抗原修复条件,让信号变强。
背景染色也很烦人,就像照片上有噪点,可能是封闭不充分、抗体非特异性结合,或者洗涤不彻底。解决办法就是优化封闭条件、选特异性高的抗体,多洗几次,洗得彻底些,让背景干净。
这些问题都得在实验中仔细排查,找到原因,才能顺利实验,得到可靠的结果。
科研实验外包 想了解更多请关注:https://www.do-gene.cn/

